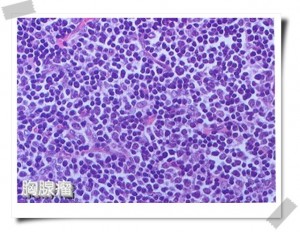
胸腺瘤是来源于胸腺上皮细胞的前纵隔常见肿瘤,其镜下表现多样,2015 版 WHO 分类将其分成5 个形态学亚型。胸腺瘤生物学行为普遍良好,大部分患者存活期可达 10 年以上,但也有少部分患者经多学科综合治疗后预后仍较差,数月内便复发转移[1]。 胸腺瘤病因尚不明确,可能与基因易感性、病毒感染等多因素相关。 因此胸腺瘤的病理诊断、治疗、预后也逐渐成为近年研究的热点。
一、病理分型及进展
2004 版WHO胸腺瘤分类是多年来用于诊断胸腺瘤的标准,先前有研究评估该分类的临床意义,但均受限于样本量不足。 2015年International Thymic Malignancy Interest Group(ITMIG)收集了全球多中心共 4 221 例胸腺瘤病例进行临床病理研究,结果显示2004 版WHO胸腺瘤分类的单因素分析与预后有关,预后由好至差分别为 A/ AB、B1、B2/ B3型,其中A 型与AB 型、B2 型与 B3 型间预后无差别[1],提示该分类具有一定的预后意义,但仍存在不少缺陷,包括可重复性较差,不同诊断结果对预后评估差异较大[16]。 新近2015年WHO胸腺瘤分类已出版,新分类仍保留了原5 种胸腺瘤类型,但增加了不典型 A 型胸腺瘤及 B3 型胸腺瘤变型,强调了各型中可区别于其他类型的关键形态学特征,丰富了免疫组织化学标志物的应用及鉴别诊断内容[2]。
- A型胸腺瘤:关键形态学特征:丰富而形态温和的梭形和卵圆形(偶尔多角形)上皮细胞;肿瘤组织中未成熟T细胞稀少或缺乏。鉴别诊断包括AB型、B3型胸腺瘤、胸腺鳞状细胞癌(TSCC)以及梭形细胞肿瘤如孤立性纤维性肿瘤和滑膜肉瘤等。当肿瘤中出现不可计数的未成熟T细胞区域或>10%的肿瘤区域具有中等数量TdT阳性T细胞浸润时,应诊断为 AB 型胸腺瘤。B3型与A型胸腺瘤鉴别的最重要形态学特征是显著的血管周围间隙(B3 型特征),局灶存在的腺体、菊形团或血管外皮瘤样结构(A 型特征)。 孤立性纤维性肿瘤与滑膜肉瘤等可利用p63、CD34、STAT6、CD56和TLE1 等免疫组织化学标志物进行鉴别。 不典型 A 型胸腺瘤变型指可表现出一定程度异型性的 A 型胸腺瘤,如细胞丰富、核分裂象增加(≥4/10 HPF)及出现局灶坏死,其预后意义尚不明确。2015年Green等[17]对12 例A/AB型胸腺瘤的研究结果显示,坏死与高侵袭性相关,而核异型及核分裂象与肿瘤侵袭性无关。
- AB 型胸腺瘤:其形态学特征为淋巴细胞稀少的A 样区域及富于淋巴细胞的B样区域交错排列;上皮细胞形态温和,呈梭形或卵圆形(偶尔多角形);灶性或弥漫分布大量未成熟T细胞。鉴别诊断包括A型、B1型和微结节型胸腺瘤。B1型类似正常胸腺,具有高度器官化、TdT 阳性的皮质区及常含有胸腺小体的髓质结构,上皮细胞网纤细且CD20阴性。 微结节型含有大量CD20阳性B细胞,上皮细胞排列成结节样,淋巴细胞分布于结节外非上皮细胞的间质中。
- B1 型胸腺瘤:其关键形态学特征为类似于未退化的正常胸腺皮质;总是存在髓质分化区。鉴别诊断包括 AB 型和B2 型胸腺瘤,胸腺增生及 T淋巴母细胞淋巴瘤(T- LBL)。B2 型上皮细胞较 B1 型丰富且成簇出现,少见髓质分化区,但血管周围间隙(PVS)常见。 与胸腺增生相比,B1 型的小叶更大、纤维包膜更厚,具有纤维间隔,皮质区占优势,髓质中极少或没有胸腺小体,上皮细胞 AIRE 阳性。 T- LBL 中皮髓质结构消失,常有幼稚淋巴细胞浸润间隔和纵隔脂肪,T 细胞受体基因重排常为单克隆性。
- B2 型胸腺瘤:其关键形态学特征为多角形上皮细胞成簇出现(≥3 个细胞);大量未成熟 T细胞混杂其中。鉴别诊断包括 B1 型和 B3 型胸腺瘤,TSCC 及 T- LBL。 B3 型胸腺瘤上皮细胞实性成片,未成熟 T 细胞稀少,但偶尔可见形态介于B2 型和 B3 型间的交界性病例,早前提出的 PVS 与细胞核大小不能作为鉴别特征。 少数 B2 型胸腺瘤伴有间变特征时需与 TSCC 鉴别,但分叶状结构、TdT 阳性 T 细胞、PVS以及缺乏 CD5/ CD117 阳性表达可与之鉴别。
- B3 型胸腺瘤:其关键形态学特征为多角形上皮细胞为主,呈实性片状生长,HE 染色低倍下呈现为红色区域;混有稀少未成熟T细胞。鉴别诊断包括B2 型胸腺瘤及TSCC。后者缺乏分叶状结构,呈浸润性生长,明显促纤维组织增生,缺乏 PVS、TdT 阳性 T 细胞、更明显的核异型以及常见细胞间桥,约 80%的病例表达 CD5 及 CD117。 B3 型胸腺瘤变型:上皮细胞可灶性呈梭形,或伴有间变特征,这些特殊的病例仍具有 B3 型胸腺瘤的典型特征(TdT 阳性 T 细胞,PVS,分叶状结构,缺乏 CD5/ CD117 表达以及常缺乏促纤维组织增生)。 部分病例形态类似B3 型胸腺瘤,缺乏 TSCC 的典型特征(核异型以及细胞间桥),但表达 CD5 和/ 或 CD117,缺乏 TdT 阳性 T细胞,该类病例在 ITMIG 的文献中建议暂时命名为“界于 B3/ TSCC 之间的交界性胸腺上皮肿瘤”,当该类病例具有明显核异型时,应诊断为“具有器官样特征的TSCC”[18]。
- 胸腺瘤免疫组织化学标志物的应用:2015 版 WHO胸腺瘤分类中增添了部分标志物的表达情况,归纳如下:PAX- 8、FOXN1、CD205、p63 在各型胸腺瘤中均有表达,可用于鉴别其他前纵隔肿瘤;胸腺皮质和髓质分化标志物(CD40、claudin 4、AIRE、HLA calss Ⅱ、thymoproteasome)常见于AB 型、B1 型、B2 型中表达;除 AB 型外,胸腺终末上皮分化标志物 ( involucrin、 CK10 ) 在其余各型中均有表达;GLUT1、MUC1 在 TSCC 中的阳性比例较B3 型高。
- 其他具有鉴别诊断意义免疫标志物的研究进展:近年研究显示,蛋白酶β5t亚单位(β5t)、desmoglein 3(DSG3)、Notch1 胞内段蛋白(N1ICD)在胸腺瘤的鉴别诊断中具有一定价值。β5t 是一种仅存于胸腺的蛋白酶体亚单位,研究显示β5t 在所有胸腺癌(31例)及非胸腺肿瘤病例中均为阴性,而在胸腺瘤中阳性率为74%,可用于鉴别胸腺瘤与其他纵隔肿瘤[19]。 糖蛋白DSG-3是桥粒中的重要成分,常在肺鳞癌中表达,研究显示83%的胸腺癌可见DSG-3表达,与之相比胸腺瘤中仅13%为阳性,因此DSG-3可用于鉴别胸腺瘤与胸腺癌[20]。富含淋巴细胞的胸腺瘤与 T- LBL 一般使用角蛋白染色进行鉴别,胸腺瘤可见角蛋白阳性的胸腺上皮细胞混杂于未成熟的淋巴样细胞中,但穿刺活检中因可能含有大量淋巴细胞而上皮细胞较少,鉴别诊断困难,研究提示表达于淋巴细胞上的 N1ICD 可用于协助诊断该类病例。Jegalian等[21]研究显示胸腺瘤中 N1ICD 表达均为1 +,而T- LBL病例则为2 +~4 +,提示 N1ICD 具有良好的鉴别意义。有学者探讨了常用标志物 Ki- 67 在协助胸腺瘤分型中的实用性,指出 Ki- 67 阳性指数 <2%的病例更倾向于 A 型胸腺瘤,介于5.1% ~13. 5%之间倾向于 B3 型胸腺瘤,>13. 5%则倾向于胸腺癌[22],结合 Ki-67阳性指数对胸腺瘤的分型有助于提高诊断的可重复性。
二、治疗
- 病理分期对治疗的影响:目前病理分期主要采用Masaoka- Koga 系统,对临床处理有较大的指导意义。2011年ITMIG 对该分期进行了更新与补充,强调Ⅱ/ Ⅲ期的诊断需要有镜下侵袭灶作依据[23],不能仅凭外科医师的肉眼观察。手术切除是胸腺瘤的首选治疗方式。对于Ⅱ ~Ⅳ期或镜下存在手术残留的胸腺瘤,应进行术后放疗。对于肉眼下存在手术残留(或无法进行手术切除)的患者,应在放疗基础上酌情进行化疗。胸腺瘤的化疗首选方案为顺铂、阿霉素、环磷酰胺(CAP)。 最新NCCN指南表明,不同 WHO 病理分型对胸腺瘤治疗的选择无影响,但不同肿瘤分期、胸腺瘤与胸腺癌间的治疗差异较大[24]。
- 靶向治疗进展:研究者已对胸腺瘤进行了不少药物临床试验,药物靶点包括 EGFR、IGF- 1R、VEGFR、组蛋白去乙酰化酶等。其中以 IGF- 1R为靶点的cixutumumab 在针对复发性胸腺瘤患者进行的Ⅱ期临床试验结果显示,14%(5/ 37)的患者达到部分缓解[25]。其余药物临床试验效果不佳,仅个别病例出现疗效。 新近研究提示 PD- L1 有望成为胸腺瘤新的治疗靶点。程序性死亡受体1 (PD- 1)及其配体PD-L1是CD28/ B7超家族成员,广泛表达于各种组织,根据机体内炎性改变程度、免疫状态和遗传背景不同而激活或抑制,可参与T 细胞的中枢及外周免疫耐受。 在肿瘤中,PD- 1/PD- L1 通路与肿瘤细胞免疫监控有关。 当表达于肿瘤特异性T细胞的 PD- 1 与表达于肿瘤细胞的 PD- L1 结合时,可促进肿瘤细胞免疫逃逸,因此肿瘤细胞 PD- L1 过表达有利于肿瘤进展。 研究显示,PD- L1 在多种肿瘤中出现过表达,相关抑制剂临床试验效果良好。
综上所述,胸腺瘤是一类主要呈惰性生长的纵隔肿瘤,小部分病例预后差,值得引起重视。 胸腺瘤 WHO 分类的更新改善了诊断重复性差的情况,但仍需研究资料验证其临床意义。 胸腺瘤的分子研究以及相关靶向治疗的临床试验正在火热开展中,必将促进对胸腺瘤分子病理学特征的深入理解以及治疗和预后预测的进步。
摘自 中华病理学杂志 2015 年 9 月第 44 卷第 9 期 作者:苏家俊 陈玉 徐方平 刘艳辉
 李文华的博客
李文华的博客